Viết Hai Phương Trình Phản Ứng Điều Chế Etilen, Tính Chất Hóa Học Và Ứng Dụng Etilen Như Thế Nào
Bài 32. Luyện tập chương 3: Phi kim – Sơ lược về bảng tuần hoàn các nguyên tố hoá học
Bài 33. Thực hành: Tính chất hóa học của phi kim và hợp chất của chúng
CHƯƠNG 4: HIĐROCACBON. NHIÊN LIỆU
Bài 34. Khái niệm về hợp chất hữu cơ và hoá học hữu cơ
Bài 35. Cấu tạo phân tử hợp chất hữu cơ
Bài 36. Metan
Bài 37. Etilen
Bài 38. Axetilen
Bài 39. Benzen
Bài 40. Dầu mỏ và khí thiên nhiên
Bài 41. Nhiên liệu
Bài 42. Luyện tập chương 4: Hiđrocacbon. Nhiên liệu
Bài 43. Thực hành: Tính chất của Hiđrocacbon
CHƯƠNG 5: DẪN XUẤT CỦA HIĐROCACBON. POLIME
Bài 44. Rượu etylic
Bài 45. Axit axetic
Bài 46. Mối liên hệ giữa etilen, rượu etylic và axit axetic
Bài 47. Chất béo
Bài 48.
Đang xem: Viết hai phương trình phản ứng điều chế etilen
Xem thêm: Giải Hệ Phương Trình 2 Ẩn Bậc 2 Lớp 10, Cách Giải Hệ Phương Trình Bậc Hai 2 Ẩn
Xem thêm: Chuyển File Xml Thành File Excel Miễn Phí Mới Nhất 2020, Cách Chuyển File Xml Sang Excel Nhanh Chóng
Luyện tập rượu etylic, axit axetic và chất béo
Bài 49. Thực hành: Tính chất của rượu và axit
Bài 50. Glucozơ
Bài 51. Saccarozơ
Bài 52. Tinh bột và xenlulozơ
Bài 53. Protein
Bài 54. Polime
Bài 55. Thực hành: Tính chất của gluxit
Bài 56. Ôn tập cuối năm
Etilen – Khái niệm, tính chất và các phản ứng điều chế quan trọng
Bài học hôm nay chúng ta cùng tìm hiểu về etilen và các tính chất hóa học cũng nhưứng dụngcủa nó là ra sao, tất cả sẽ được giải đáp trong bài viết hôm nay!
I. Khái quát chung
1. Etilen là gì?
Etilen là một trong những hydrocacbon phổ biến thuộc dãy đồng đẳng của ankan, với đặc tính nhận biết chính là ít tan trong nước nhưng tan nhiều trong ete và một số dung dịch hữu cơ khác. Công thức hóa học của etile là:(CH_2=CH_2)hay(C_2H_4)
| Danh pháp IUPAC | Ethene |
| Công thức hoá học | C2H4 |
| SMILES | C=C |
| Phân tử khối | 28,05 g/mol |
| Bề ngoài | khí không màu |
| Tỷ trọngvàpha | 1,178 g/l ở 15°C, gas |
| Độ hoà tancủa khí trongnước | 25 mL/100 mL (0°C) 12 mL/100 mL (25°C)<1> |
| Nhiệt độ nóng chảy | -103,7°C |
Mới nhất:
II. Tính chất hóa học
Phản ứng cộng
Phản ứngvớiHalogen:
– Etilen + Br2 :(C_2H_4 +Br_2
ightarrow C_2H_4Br_2)
– Tác dụng vớiH2:(C_2H_4 +H_2
ightarrow C_2H_6)
– Tác dụng vớivớiaxit:(C_2H_4 + HBr
ightarrow C_2H_5Br)
Phản ứng trùng hợp etilen (xúc tác nhiệt độ)
| (nCH_2=CH_2) | → | ((-CH_2-CH_2-)n) |
| (khí) | (rắn) | |
| (không màu) |
Etilen + KMnO4
(3C_2H_4 + 2KMnO_4 + 4H_2O
ightarrow 3C_2H_5(OH)_2 + 2KOH + 2MnO_2)
Phản ứng cháy
Phương trình:
(C_2H_4 + 3O_2 {displaystyle longrightarrow } 2CO_2 + 2H_2O)
Etilen tác dụng với brom
Làm đổi màu dung dịch brom
Mối liên hệ giữa etilen rượu etylic và axit axetic.
Etilen là chất giúp tạo ra rượu etylic và axit axetic. Phương trình hóa học như sau:
(C_2H_4
ightarrow <+H_2O,xt>CH_3-CH_2-OH
ightarrow <+O_2, men>CH_3COOH)
(C_2H_4+H_2O
ightarrow
(C_2H_5OH+O_2
ightarrow <+O_2, men>CH_3COOH+H_2O)
III. Điều chế etilen
Điều chế từ ancol etylic ra etilen
Cho (H_2SO_4) đặc vào rượu etylic, đun nóng:
(C_2H_5OH
ightarrow C_2H_4 + H_2O )
Điều chế từ axetilen ra etilen
Tạo khí (C_2H_2), sau đó cho xúc tác với chỉ hoặc paradiltác dụng với H_2
(CaC_2 + 2H_2O
ightarrow Ca(OH)_2 + C_2H_2 )
(C_2H_2 + H_2
ightarrow C_2H_4) ( điều kiện: (Pd/ Pb,) đun nóng)
IV. Ứng dụng của etilen
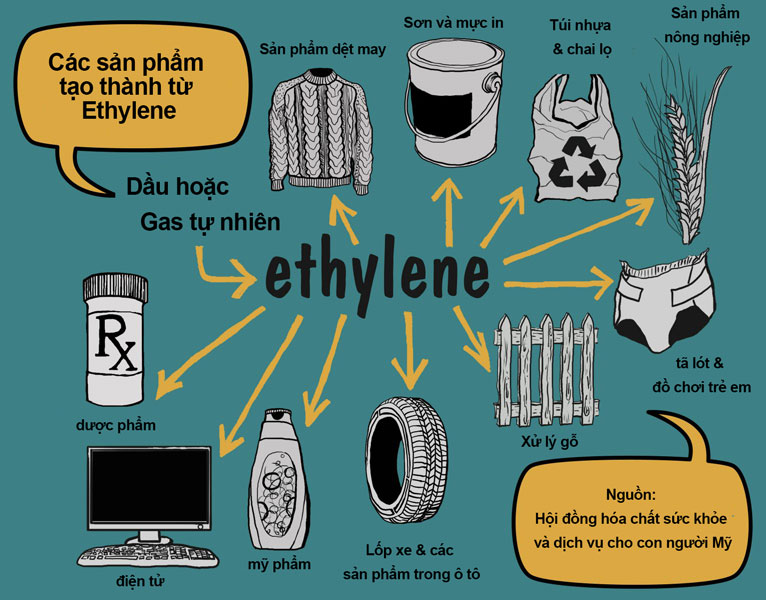
Etilen là một chất hóa học được sử dụng rộng rãi đặc biệt là trong sản xuất polime. Một số sản phẩm từ etilen như sau:
Bao bì. Dệt ma Vận chuyển Công nghiệp xây dựng Điện tử Chất phủ và chất kết dính. Hóa chất tiêu dùng
Với những lý thuyết bổ ích trên hy vọng các bạn đã hiểu được tính chất hóa học vài bài tập về etilen. Nếu còn thắc mắc xin vui lòng để lại dưới mục bình luận. Chúc các bạn học vui và đừng quên follow trang web nhé!